kleinste Einheit eines chemischen Elements
| Heliumatom | |
|---|---|
 Eine Abbildung des Heliumatoms, die den Kern (pink) und die Elektronenwolkenverteilung (schwarz) darstellt. Der Kern (oben rechts) in Helium-4 ist in Wirklichkeit kugelsymmetrisch und ähnelt stark der Elektronenwolke, obwohl dies für kompliziertere Kerne nicht immer der Fall ist. Der schwarze Balken ist ein Angström ( 10 -10 m oder 100 pm 100 pm ] Kleinste erkannte Aufteilung eines chemischen Elements | |
| Eigenschaften | |
| Massenbereich | 1.67 × 10 −27 [1965901200] 4,52 × 10 −25 kg |
| Elektrische Ladung | Null (neutral) oder Ionenladung |
| Durchmesser | 62 pm (He ) bis 520 pm (Cs) (Datenseite) |
| Komponenten | Elektronen und ein kompakter Kern aus Protonen und Neutronen |
Ein -Atom ist die kleinste konstituierende Einheit der gewöhnlichen Materie, die die Eigenschaften besitzt eines chemischen Elements. Jeder Feststoff, jede Flüssigkeit, jedes Gas und jedes Plasma besteht aus neutralen oder ionisierten Atomen. Atome sind extrem klein; Typische Größen sind etwa 100 Pikometer (ein Zehnmilliardstel Meter in der kurzen Skala).
Atome sind so klein, dass der Versuch, ihr Verhalten mithilfe der klassischen Physik vorherzusagen, als ob sie Billiardkugeln wären, aufgrund von Quanteneffekten deutlich falsche Vorhersagen liefert. Durch die Entwicklung der Physik haben atomare Modelle Quantenprinzipien eingeführt, um dieses Verhalten besser erklären und vorhersagen zu können.
Jedes Atom besteht aus einem Kern und einem oder mehreren an den Kern gebundenen Elektronen. Der Kern besteht aus einem oder mehreren Protonen und typischerweise einer ähnlichen Anzahl von Neutronen. Protonen und Neutronen werden als Nukleonen bezeichnet. Über 99,94% der Masse eines Atoms befinden sich im Kern. Die Protonen haben eine positive elektrische Ladung, die Elektronen haben eine negative elektrische Ladung und die Neutronen haben keine elektrische Ladung. Wenn die Anzahl der Protonen und Elektronen gleich ist, ist dieses Atom elektrisch neutral. Wenn ein Atom mehr oder weniger Elektronen als Protonen hat, dann hat es eine negative oder positive Gesamtladung und wird Ion genannt.
Durch diese elektromagnetische Kraft werden die Elektronen eines Atoms von den Protonen in einem Atomkern angezogen. Die Protonen und Neutronen im Kern werden von einer anderen Kraft, der Kernkraft, angezogen, die normalerweise stärker ist als die elektromagnetische Kraft, die die positiv geladenen Protonen voneinander abstößt. Unter bestimmten Umständen wird die abstoßende elektromagnetische Kraft stärker als die Kernkraft, und Nukleonen können aus dem Kern herausgeschleudert werden, wodurch ein anderes Element zurückbleibt: Kernzerfall, der zu einer Kerntransmutation führt.
Die Anzahl der Protonen im Kern bestimmt, zu welchem chemischen Element das Atom gehört: Zum Beispiel enthalten alle Kupferatome 29 Protonen. Die Anzahl der Neutronen definiert das Isotop des Elements. Die Anzahl der Elektronen beeinflusst die magnetischen Eigenschaften eines Atoms. Atome können durch chemische Bindungen an ein oder mehrere andere Atome gebunden werden, um chemische Verbindungen wie Moleküle zu bilden. Die Fähigkeit von Atomen, sich zu assoziieren und zu dissoziieren, ist für die meisten physikalischen Veränderungen verantwortlich, die in der Natur beobachtet werden, und ist Gegenstand der Disziplin der Chemie.
Geschichte der Atomtheorie
Atome in der Philosophie
Die Idee, dass Materie aus diskreten Einheiten besteht, ist eine sehr alte Idee, die in vielen alten Kulturen wie Griechenland und Indien auftaucht. Das Wort "atom" (griechisch: ἄτομος ; atomos ), was "unbeschneidbar" bedeutet, wurde von den antiken griechischen Philosophen Leucippus und seinem Schüler Democritus (ca. 19459037) 460 geprägt. c. 370 v. Chr.] [1][2][3][4] Democritus lehrte, dass die Anzahl der Atome unendlich groß, ungebildet und ewig sei und dass die Eigenschaften eines Objekts sich aus der Art der Atome ergeben, aus denen es besteht. [2][3][4] Democritus Der Atomismus wurde vom späteren Philosophen Epicurus (341–270 v. Chr.) verfeinert und weiterentwickelt. [3][4] Während des frühen Mittelalters wurde der Atomismus in Westeuropa größtenteils vergessen, überlebte jedoch bei einigen Gruppen islamischer Philosophen. [3] Während des 12. Jahrhunderts wurde der Atomismus in Westeuropa durch Anspielungen in den wiederentdeckten Schriften von Aristoteles erneut bekannt. [3]
Im 14. Jahrhundert wurde die Wiederentdeckung wichtiger Werke, die atomistische Lehren beschreiben, einschließlich der von Lucretius De rerum natura [19459] 036] und Diogenes Laërtius ' Leben und Meinungen bedeutender Philosophen führten zu einer verstärkten wissenschaftlichen Beachtung des Themas. [3] Nichtsdestoweniger, weil der Atomismus mit der Philosophie des Epikuräismus in Verbindung gebracht wurde, in der der Glaube an die orthodoxen christlichen Lehren widersprach Atome galten nicht als akzeptabel. [3] Der französische katholische Priester Pierre Gassendi (1592–1655) belebte den epikureischen Atomismus mit Modifikationen. Er argumentierte, dass Atome von Gott geschaffen wurden und, obwohl sie äußerst zahlreich sind, nicht unendlich sind. [3][4] Gassendis modifizierte Theorie von Die Atome wurden in Frankreich durch den Arzt François Bernier (1620–1688) und in England durch den Naturphilosophen Walter Charleton (1619–1707) populär gemacht. [3] Der Chemiker Robert Boyle (1627–1691) und der Physiker Isaac Newton (1642– 1727) verteidigten den Atomismus und waren Ende des 17. Jahrhunderts von Teilen der wissenschaftlichen Gemeinschaft akzeptiert worden. [3]
Erste evidenzbasierte Theorie

In den frühen 1800er Jahren erklärte John Dalton das Konzept der Atome, um zu erklären, warum Elemente immer in kleinen Verhältnissen reagieren ganze Zahlen (das Gesetz der mehrfachen Proportionen). Zum Beispiel gibt es zwei Arten von Zinnoxid: Eine besteht aus 88,1% Zinn und 11,9% Sauerstoff und die andere besteht aus 78,7% Zinn und 21,3% Sauerstoff (Zinn (II) oxid bzw. Zinndioxid). Dies bedeutet, dass sich 100 g Zinn entweder mit 13,5 g oder 27 g Sauerstoff verbinden. 13,5 und 27 bilden ein Verhältnis von 1: 2, ein Verhältnis von kleinen ganzen Zahlen. Dieses in der Chemie übliche Muster deutete Dalton an, dass Elemente in Vielfachen von diskreten Einheiten - also Atomen - reagieren. Im Fall von Zinnoxiden verbindet sich ein Zinnatom entweder mit einem oder zwei Sauerstoffatomen. [5]
Dalton glaubte auch, dass die Atomtheorie erklären könnte, warum Wasser unterschiedliche Gase in unterschiedlichen Anteilen absorbiert. Er fand zum Beispiel, dass Wasser Kohlendioxid weit besser absorbiert als Stickstoff. [6] Dalton vermutete, dass dies auf die Unterschiede zwischen den Massen und Konfigurationen der jeweiligen Gase-Partikel und der Kohlendioxidmoleküle zurückzuführen sei (CO 2) ) sind schwerer und größer als Stickstoffmoleküle (N 2 ).
Brownsche Bewegung
Im Jahr 1827 nutzte der Botaniker Robert Brown ein Mikroskop, um im Wasser schwebende Staubkörner zu betrachten, und entdeckte, dass sie sich unregelmäßig bewegten, ein Phänomen, das als "Brownsche Bewegung" bekannt wurde. Es wurde angenommen, dass dies durch Wassermoleküle verursacht wurde, die die Körner herumstoßen. 1905 bewies Albert Einstein die Realität dieser Moleküle und ihrer Bewegungen, indem er die erste statistische Physikanalyse der Brownschen Bewegung erstellte. [7][8][9] Der französische Physiker Jean Perrin nutzte Einsteins Arbeit, um experimentell Masse und Abmessungen von Atomen zu bestimmen und damit Daltons Atomatom endgültig zu überprüfen Theorie. [10]
Entdeckung des Elektrons

Oben: Erwartete Ergebnisse: Alphateilchen durchlaufen das Plumpuddingmodell des Atoms mit vernachlässigbarer Auslenkung.
Bottom : Beobachtete Ergebnisse: Ein kleiner Teil der Teilchen wurde durch die konzentrierte positive Ladung des Kerns abgelenkt.
Der Physiker JJ Thomson maß die Masse der Kathodenstrahlen und zeigte, dass sie aus Partikeln bestehen, aber um das 1800-fache leichter waren als das leichteste Atom, Wasserstoff. Daher waren sie keine Atome, sondern ein neues Teilchen, das erste zu entdeckende subatomare -Partikel, das er ursprünglich " corpuscle " nannte, später jedoch als electron bezeichnet wurde. Nach den von George Johnstone Stoney im Jahr 1874 postulierten Partikeln zeigte er auch, dass sie identisch mit Partikeln sind, die von photoelektrischen und radioaktiven Stoffen abgegeben werden. [11] Es wurde schnell erkannt, dass es sich um Partikel handelt, die elektrische Ströme in Metalldrähten transportieren und die Partikel transportieren negative elektrische Ladung innerhalb der Atome. Thomson erhielt für diese Arbeit den Nobelpreis für Physik von 1906. So warf er den Glauben auf, dass Atome die unteilbaren, ultimativen Teilchen der Materie sind. [12] Thomson postulierte auch fälschlicherweise, dass die negativ geladenen Elektronen mit niedriger Masse in einem einheitlichen Meer positiver Ladung im Atom verteilt waren. Dies wurde als Plumpudding-Modell bekannt.
Entdeckung des Zellkerns
1909 bombardierten Hans Geiger und Ernest Marsden unter der Leitung von Ernest Rutherford eine Metallfolie mit Alphateilchen, um deren Streuung zu beobachten. Sie erwarteten, dass alle Alphateilchen mit geringer Ablenkung direkt durchlaufen würden, da das Modell von Thomson sagte, die Ladungen im Atom seien so diffus, dass ihre elektrischen Felder die Alphateilchen nicht sehr stark beeinflussen könnten. Geiger und Marsden entdeckten jedoch, dass Alphateilchen um Winkel von mehr als 90 ° abgelenkt wurden, was laut Thomson-Modell unmöglich sein sollte. Um dies zu erklären, schlug Rutherford vor, dass die positive Ladung des Atoms in einem kleinen Kern im Zentrum des Atoms konzentriert ist. [13]
Entdeckung von Isotopen
Beim Experimentieren mit den Produkten des radioaktiven Zerfalls entdeckte 1913 der Radiochemiker Frederick Soddy an jeder Position des Periodensystems schien es mehr als eine Art von Atom zu geben. [14] Der Begriff Isotop wurde von Margaret Todd als geeigneter Name für verschiedene Atome, die zu demselben Element gehören, geprägt. J.J. Thomson entwickelte eine Methode zur Isotopentrennung durch seine Arbeit an ionisierten Gasen, die anschließend zur Entdeckung stabiler Isotope führte. [15]
Bohr-Modell
1913 schlug der Physiker Niels Bohr ein Modell vor, bei dem angenommen wurde, dass die Elektronen eines Atoms den Kern umkreisen, dies aber nur in einer begrenzten Anzahl von Umlaufbahnen tun könnten und nur zwischen diesen Umlaufbahnen springen könnten diskrete Energieänderungen entsprechend der Absorption oder Strahlung eines Photons. [16] Diese Quantisierung wurde verwendet, um zu erklären, warum die Elektronenbahnen stabil sind (da Beschleunigungen, einschließlich Kreisbewegung, normalerweise kinetische Energie verlieren, die als elektromagnetische Strahlung abgegeben wird) siehe Synchrotronstrahlung ) und warum Elemente elektromagnetische Strahlung in diskreten Spektren absorbieren und emittieren. [17]
Später im selben Jahr lieferte Henry Moseley zusätzliche experimentelle Beweise für Niels Bohrs Theorie. Diese Ergebnisse verfeinerten das Modell von Ernest Rutherford und Antonius Van den Broek, in dem vorgeschlagen wurde, dass das Atom in seinem Kern eine Anzahl positiver Kernladungen enthält, die der (Atom-) Zahl im Periodensystem entspricht. Bis zu diesen Versuchen war die Ordnungszahl nicht als physikalische und experimentelle Größe bekannt. Dass es der atomaren Kernladung entspricht, bleibt bis heute das akzeptierte Atommodell. [18]
Chemische Bindung erklärt
Chemische Bindungen zwischen Atomen wurden jetzt von Gilbert Newton Lewis (1916) als Wechselwirkungen zwischen ihren konstituierenden Elektronen erklärt. [19659066] Da bekannt war, dass sich die chemischen Eigenschaften der Elemente nach dem periodischen Gesetz weitgehend wiederholten, [20] schlug der amerikanische Chemiker Irving Langmuir 1919 vor, dies könne erklärt werden, wenn die Elektronen in einem Atom auf irgendeine Weise verbunden oder gebündelt würden. Es wurde angenommen, dass Elektronengruppen eine Reihe von Elektronenhüllen um den Kern besetzen. [21]
Weiterentwicklungen in der Quantenphysik
Das Stern-Gerlach-Experiment von 1922 lieferte weitere Hinweise auf die Quantennatur atomarer Eigenschaften. Wenn ein Strahl von Silberatomen durch ein speziell geformtes Magnetfeld geführt wurde, wurde der Strahl in einer Weise aufgeteilt, die mit der Richtung des Drehimpulses oder Spin eines Atoms korrelierte. Da diese Drehrichtung anfangs zufällig ist, wird erwartet, dass der Strahl in eine zufällige Richtung abgelenkt wird. Stattdessen wurde der Strahl in zwei Richtungskomponenten aufgeteilt, die dem atomaren Spin entsprechen, der in Bezug auf das Magnetfeld nach oben oder unten ausgerichtet ist. [22]
. 1925 veröffentlichte Werner Heisenberg die erste konsistente mathematische Formulierung Quantenmechanik (Matrix Mechanics). [18] Ein Jahr zuvor, im Jahre 1924, hatte Louis de Broglie vorgeschlagen, dass alle Teilchen sich wie Wellen verhalten sollten, und 1926 nutzte Erwin Schrödinger diese Idee, um ein mathematisches Modell des Atoms zu entwickeln (Wave Mechanics), in dem die Elektronen als dreidimensionale Wellenformen und nicht als Punktpartikel beschrieben wurden.
Die Verwendung von Wellenformen zur Beschreibung von Partikeln hat zur Folge, dass es mathematisch unmöglich ist, genaue Werte für die Position und den Impuls eines Partikels zu einem bestimmten Zeitpunkt zu erhalten. dies wurde als das Unbestimmtheitsprinzip bekannt, das Werner Heisenberg 1927 formulierte. [18] Bei diesem Konzept konnte man für eine gegebene Genauigkeit bei der Messung einer Position nur einen Bereich wahrscheinlicher Werte für das Moment erhalten und umgekehrt. [23]
This Das Modell konnte Beobachtungen des atomaren Verhaltens erklären, die bei früheren Modellen nicht möglich waren, z. B. bestimmte Struktur- und Spektralmuster von Atomen, die größer als Wasserstoff sind. Daher wurde das Planetenmodell des Atoms zugunsten eines solchen verworfen, in dem Atomorbitalzonen um den Kern beschrieben wurden, in denen am ehesten ein Elektron beobachtet werden kann. [24][25]
Entdeckung des Neutrons
Die Entwicklung des Massenspektrometers war möglich die Masse der Atome mit erhöhter Genauigkeit gemessen werden. Die Vorrichtung verwendet einen Magneten, um die Flugbahn eines Ionenstrahls zu biegen, und das Ausmaß der Ablenkung wird durch das Verhältnis der Masse eines Atoms zu seiner Ladung bestimmt. Der Chemiker Francis William Aston benutzte dieses Instrument, um zu zeigen, dass Isotope unterschiedliche Massen hatten. Die Atommasse dieser Isotope variierte um ganzzahlige Beträge, die Ganzzahlregel. [26] Die Erklärung für diese verschiedenen Isotope erwartete die Entdeckung des Neutrons, eines ungeladenen Teilchens mit einer dem Proton ähnlichen Masse, durch den Physiker James Chadwick 1932. Isotope wurden dann als Elemente mit der gleichen Anzahl von Protonen, jedoch unterschiedlichen Anzahlen von Neutronen im Kern erklärt. [27]
Spaltung, Hochenergiephysik und kondensierte Materie
Im Jahr 1938 war der deutsche Chemiker Otto Hahn ein Student von Rutherford richteten Neutronen auf Uranatome, die erwarteten, Transuranelemente zu erhalten. Stattdessen zeigten seine chemischen Experimente Barium als Produkt. [28][29] Ein Jahr später bestätigten Lise Meitner und ihr Neffe Otto Frisch, dass Hahns Ergebnis die erste experimentelle Kernspaltung war . [30][31] 1944 erhielt Hahn der Nobelpreis für Chemie. Trotz Hahns Bemühungen wurden die Beiträge von Meitner und Frisch nicht anerkannt. 19459106 [32]
In den fünfziger Jahren ermöglichte die Entwicklung verbesserter Teilchenbeschleuniger und Teilchendetektoren den Forschern, die Auswirkungen von Atomen zu untersuchen, die sich in großer Höhe bewegen Energien. [33] Es wurde gefunden, dass Neutronen und Protonen Hadronen sind oder Verbundstoffe aus kleineren Teilchen, die als Quarks bezeichnet werden. Das Standardmodell der Teilchenphysik wurde entwickelt, das die Eigenschaften des Kerns bisher erfolgreich in Bezug auf diese subatomaren Teilchen und die Kräfte erklärt, die ihre Wechselwirkungen bestimmen. [34]
Structure
Subatomische Teilchen
Obwohl das Wort atom bezeichnete ursprünglich ein Teilchen, das nicht in kleinere Teilchen geschnitten werden kann. In der modernen wissenschaftlichen Verwendung besteht das Atom aus verschiedenen subatomaren Teilchen. Die konstituierenden Teilchen eines Atoms sind das Elektron, das Proton und das Neutron; Alle drei sind Fermionen. Das Wasserstoff-1-Atom hat jedoch keine Neutronen und das Hydronion hat keine Elektronen.
Das Elektron ist bei 9.11 × 10 -31 kg bei einer negativen elektrischen Ladung das mit Abstand geringste Gewicht und eine Größe, die zu klein ist, um unter Verwendung verfügbarer Techniken gemessen zu werden. [35] Es war das leichteste Teilchen mit einer positiven gemessenen Ruhemasse, bis die Neutrino-Masse entdeckt wurde. Unter normalen Bedingungen werden Elektronen durch die Anziehungskraft, die durch entgegengesetzte elektrische Ladungen erzeugt wird, an den positiv geladenen Kern gebunden. Hat ein Atom mehr oder weniger Elektronen als seine Ordnungszahl, so wird es insgesamt negativ oder positiv geladen; Ein geladenes Atom wird Ion genannt. Elektronen sind seit dem späten 19. Jahrhundert bekannt, hauptsächlich dank J.J. Thomson; Einzelheiten finden Sie in der Geschichte der subatomaren Physik.
Protonen haben eine positive Ladung und eine 1.836-fache Masse wie das Elektron bei 1.6726 × 10 −27 kg . Die Anzahl der Protonen in einem Atom wird als Ordnungszahl bezeichnet. Ernest Rutherford (1919) beobachtete, dass Stickstoff unter Beschuss mit Alpha-Teilchen Wasserstoff auslöst, was wie Wasserstoffkerne aussieht. Bis 1920 hatte er akzeptiert, dass der Wasserstoffkern ein bestimmtes Teilchen innerhalb des Atoms ist, und nannte es Proton.
Neutronen haben keine elektrische Ladung und haben eine freie Masse des 1,839-fachen der Masse des Elektrons, [36] oder 1.6929 × 10 10 10 -227 ] Kg das schwerste der drei konstituierenden Teilchen, kann jedoch durch die nukleare Bindungsenergie reduziert werden. Neutronen und Protonen (zusammen als Nukleonen bekannt) haben vergleichbare Abmessungen - in der Größenordnung von 2.5 × 10 -15 m m . Die Oberfläche dieser Teilchen ist nicht scharf definiert. [37] Das Neutron wurde 1932 vom englischen Physiker James Chadwick entdeckt.
Im Standardmodell der Physik sind Elektronen wahrlich Elementarteilchen ohne innere Struktur. Sowohl Protonen als auch Neutronen sind jedoch Verbundpartikel, die aus Elementarteilchen bestehen, die als Quarks bezeichnet werden. Es gibt zwei Arten von Quarks in Atomen, die jeweils eine gebrochene elektrische Ladung haben. Protonen bestehen aus zwei Up-Quarks (jeweils mit Ladung 2 / 3 ) und einem Down-Quark (mit einer Ladung von 1 /
3) ). Neutronen bestehen aus einem Up-Quark und zwei Down-Quarks. Diese Unterscheidung macht den Unterschied in Masse und Ladung zwischen den beiden Teilchen aus. [38] [39]
Die Quarks werden durch die starke Wechselwirkung (oder starke Kraft) zusammengehalten. , die durch Gluonen vermittelt wird. Die Protonen und Neutronen wiederum werden im Kern durch die Kernkraft zusammengehalten, die ein Residuum der starken Kraft ist, die etwas unterschiedliche Bereichseigenschaften hat (siehe den Artikel über die Kernkraft für weitere Informationen). Das Gluon ist ein Mitglied der Familie der Eichbosonen, bei denen es sich um Elementarteilchen handelt, die physikalische Kräfte vermitteln. [38][39]
Nukleus

Alle gebundenen Protonen und Neutronen in einem Atom bilden einen winzigen Atomkern und werden kollektiv als Nukleonen bezeichnet. Der Radius eines Kerns ist ungefähr gleich 1,07 3 √ A fm, wobei A die Gesamtzahl der Nukleonen ist. [40] Dies ist viel kleiner als der Radius des Atoms, der in der Größenordnung von 10 5 fm liegt. Die Nukleonen sind durch ein kurzreiches Anziehungspotential, die als starke Restkraft bezeichnet wird, miteinander verbunden. Bei Entfernungen von weniger als 2,5 fm ist diese Kraft viel stärker als die elektrostatische Kraft, die bewirkt, dass sich positiv geladene Protonen gegenseitig abstoßen. [41]
Atome desselben Elements haben die gleiche Anzahl von Protonen. nannte die Ordnungszahl. Innerhalb eines einzelnen Elements kann die Anzahl der Neutronen variieren, wodurch das Isotop dieses Elements bestimmt wird. Die Gesamtzahl der Protonen und Neutronen bestimmt das Nuklid. Die Anzahl der Neutronen im Verhältnis zu den Protonen bestimmt die Stabilität des Kerns, wobei bestimmte Isotope radioaktiv zerfallen. [42]
Das Proton, das Elektron und das Neutron werden als Fermionen klassifiziert. Fermionen gehorchen dem Pauli-Ausschlussprinzip, das identischen Fermionen, wie etwa mehreren Protonen, die gleichzeitige Besetzung des gleichen Quantenzustands verbietet. Somit muss jedes Proton im Kern einen Quantenzustand einnehmen, der sich von allen anderen Protonen unterscheidet, und dasselbe gilt für alle Neutronen des Kerns und für alle Elektronen der Elektronenwolke. [43]
A Ein Kern, der eine andere Anzahl von Protonen als Neutronen hat, kann möglicherweise durch einen radioaktiven Zerfall in einen Zustand niedrigerer Energie abfallen, der dazu führt, dass die Anzahl der Protonen und Neutronen enger zusammenpasst. Infolgedessen sind Atome mit übereinstimmender Anzahl von Protonen und Neutronen stabiler gegen Zerfall. Mit zunehmender Ordnungszahl erfordert die gegenseitige Abstoßung der Protonen jedoch einen zunehmenden Anteil von Neutronen, um die Stabilität des Kerns aufrechtzuerhalten, was diesen Trend der gleichen Anzahl von Protonen zu Neutronen leicht verändert. [43]

Die Anzahl der Protonen und Neutronen im Atomkern kann verändert werden, obwohl dies sehr hohe Energien erfordern kann der starken Kraft. Kernfusion tritt auf, wenn sich mehrere Atomteilchen zu einem schwereren Kern verbinden, beispielsweise durch die energetische Kollision zweier Kerne. Im Kern der Sonne benötigen Protonen beispielsweise Energien von 3–10 keV, um ihre gegenseitige Abstoßung - die Coulomb-Barriere - zu überwinden und zu einem einzigen Kern zusammenzufassen. [44] Die Kernspaltung ist der entgegengesetzte Prozess, der zur Spaltung eines Kerns führt in zwei kleinere Kerne - normalerweise durch radioaktiven Zerfall. Der Kern kann auch durch Beschuss mit hochenergetischen subatomaren Teilchen oder Photonen modifiziert werden. Verändert sich dadurch die Anzahl der Protonen in einem Kern, so ändert sich das Atom in ein anderes chemisches Element. [45] [46]
Wenn die Masse des Kerns nach einer Fusion auftritt Ist die Reaktion weniger als die Summe der Massen der einzelnen Partikel, kann die Differenz zwischen diesen beiden Werten als eine Art nutzbarer Energie (wie z. B. ein Gammastrahl oder die kinetische Energie eines Beta-Partikels) emittiert werden Die Masse-Energie-Äquivalenzformel von Albert Einstein, E = mc 2 wobei m der Massenverlust und c der ist Lichtgeschwindigkeit. Dieses Defizit ist Teil der Bindungsenergie des neuen Kerns, und es ist der nicht wiederherstellbare Verlust der Energie, der bewirkt, dass die verschmolzenen Teilchen in einem Zustand zusammen bleiben, in dem diese Energie getrennt werden muss. [47]
Die Fusion zweier Kerne, die größere Kerne mit niedrigeren Atomzahlen als Eisen und Nickel bilden (Gesamtnukleonenzahl ca. 60), ist in der Regel ein exothermer Prozess, bei dem mehr Energie freigesetzt wird, als zum Zusammenbringen erforderlich ist. [48] Dieser Energiefreisetzungsprozess macht die Kernfusion in Sternen zu einer sich selbst erhaltenden Reaktion. Für schwerere Kerne beginnt die Bindungsenergie pro Nukleon im Kern abzunehmen. Dies bedeutet, dass Fusionsverfahren, die Kerne erzeugen, die Atomzahlen größer als etwa 26 und Atommassen höher als etwa 60 aufweisen, ein endothermer Prozess sind. Diese massiveren Kerne können keine Energie erzeugende Fusionsreaktion eingehen, die das hydrostatische Gleichgewicht eines Sterns aufrechterhalten kann. [43]
Elektronenwolke
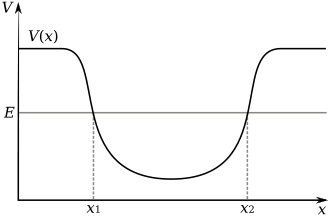
Die Elektronen In einem Atom werden die Protonen im Kern durch die elektromagnetische Kraft angezogen. Diese Kraft bindet die Elektronen in einem elektrostatischen Potentialtopf, der den kleineren Kern umgibt, was bedeutet, dass eine externe Energiequelle erforderlich ist, damit das Elektron entweichen kann. Je näher ein Elektron am Kern ist, desto größer ist die Anziehungskraft. Daher benötigen Elektronen, die in der Nähe des Zentrums des Potentialtopfes gebunden sind, mehr Energie zum Entweichen als bei größeren Abständen.
Elektronen haben wie andere Teilchen Eigenschaften sowohl eines Teilchens als auch einer Welle. Die Elektronenwolke ist eine Region innerhalb der Potenzialmulde, in der jedes Elektron eine Art dreidimensionaler stehender Welle bildet - eine Wellenform, die sich nicht relativ zum Kern bewegt. Dieses Verhalten wird durch ein Atomorbital definiert, eine mathematische Funktion, die die Wahrscheinlichkeit charakterisiert, mit der ein Elektron sich an einem bestimmten Ort befindet, wenn seine Position gemessen wird. [49] Um den Kern gibt es nur eine diskrete (oder quantisierte) Menge dieser Orbitale da andere mögliche Wellenmuster schnell in eine stabilere Form zerfallen. [50] Orbitale können eine oder mehrere Ring- oder Knotenstrukturen aufweisen und unterscheiden sich in Größe, Form und Orientierung. [51]

Jedes Atomorbital entspricht einem bestimmten Energieniveau des Elektrons. Das Elektron kann seinen Zustand auf ein höheres Energieniveau ändern, indem es ein Photon mit ausreichend Energie absorbiert, um es in den neuen Quantenzustand zu bringen. In ähnlicher Weise kann ein Elektron in einem höheren Energiezustand durch spontane Emission in einen Zustand niedrigerer Energie abfallen, während die überschüssige Energie als Photon abgestrahlt wird. Diese charakteristischen Energiewerte, definiert durch die Unterschiede in den Energien der Quantenzustände, sind für atomare Spektrallinien verantwortlich. [50]
Die Energiemenge, die zum Entfernen oder Hinzufügen eines Elektrons - des Elektrons - benötigt wird Bindungsenergie - ist weit weniger als die Bindungsenergie von Nukleonen. Zum Beispiel sind nur 13,6 eV erforderlich, um ein Elektron im Grundzustand von einem Wasserstoffatom zu entfernen, [52] im Vergleich zu 2,23 Millionen eV für die Spaltung eines Deuteriumkerns. [53] Atome sind elektrisch neutral, wenn dies der Fall ist eine gleiche Anzahl von Protonen und Elektronen. Atome, die entweder ein Defizit oder einen Überschuss an Elektronen haben, werden als Ionen bezeichnet. Elektronen, die am weitesten vom Kern entfernt sind, können auf andere Atome in der Nähe übertragen oder von Atomen geteilt werden. Durch diesen Mechanismus können sich Atome an Moleküle und andere Arten chemischer Verbindungen wie ionische und kovalente Netzwerkkristalle binden. [54]
Eigenschaften
Nukleare Eigenschaften
Definitionsgemäß zwei beliebige Atome mit einer identischen Anzahl von Protonen in ihren Kernen gehören zu demselben chemischen Element. Atome mit gleicher Anzahl von Protonen, aber einer unterschiedlichen Anzahl von -Neutronen sind verschiedene Isotope desselben Elements. Zum Beispiel lassen alle Wasserstoffatome genau ein Proton zu, aber Isotope existieren ohne Neutronen (Wasserstoff-1, bei weitem die häufigste Form, [55] auch Protium genannt), ein Neutron (Deuterium), zwei Neutronen (Tritium) und mehr als zwei Neutronen. Die bekannten Elemente bilden eine Reihe von Ordnungszahlen, vom einzelnen Protonenelement Wasserstoff bis zum 118-Protonenelement. [56] Alle bekannten Isotope von Elementen mit Ordnungszahlen größer als 82 sind radioaktiv, obwohl die Radioaktivität von Element 83 (Wismut ) ist so gering, dass es praktisch vernachlässigbar ist. [57] [58]
Etwa 339 Nuklide kommen natürlicherweise auf der Erde vor, [59] davon 254 (etwa 75%). Es wurde kein Zerfall beobachtet und als "stabile Isotope" bezeichnet. Allerdings sind nur 90 dieser Nuklide selbst theoretisch gegen jeden Zerfall stabil. Es wurde nicht beobachtet, dass weitere 164 (die Gesamtzahl auf 254 erhöht) zerfallen, obwohl dies theoretisch energetisch möglich ist. Diese werden auch formal als "stabil" eingestuft. Weitere 34 radioaktive Nuklide haben Halbwertszeiten von mehr als 80 Millionen Jahren und sind langlebig genug, um von der Geburt des Sonnensystems anwesend zu sein. Diese Ansammlung von 288 Nukliden ist als Ur-Nuklide bekannt. Es ist bekannt, dass weitere 51 kurzlebige Nuklide natürlicherweise als Tochterprodukte des primordialen Nuklidzerfalls (wie Radium aus Uran) oder als Produkte natürlicher energetischer Prozesse auf der Erde (z. B. Beschuss mit kosmischen Strahlen) (z. B. Kohlenstoff-14) [60] [note 1]
Für 80 der chemischen Elemente existiert mindestens ein stabiles Isotop. In der Regel gibt es für jedes dieser Elemente nur eine Handvoll stabile Isotope, wobei der Durchschnitt 3,2 stabile Isotope pro Element ist. Sechsundzwanzig Elemente haben nur ein einziges stabiles Isotop, während für jedes Element die größte Anzahl stabiler Isotope zehn ist, für das Element Zinn. Die Elemente 43, 61 und alle Elemente mit der Nummer 83 oder höher haben keine stabilen Isotope. [61] Seite benötigt ]
Die Stabilität von Isotopen wird durch das Verhältnis von Protonen zu Neutronen beeinflusst auch durch das Vorhandensein bestimmter "magischer Zahlen" von Neutronen oder Protonen, die geschlossene und gefüllte Quantenschalen darstellen. Diese Quantenschalen entsprechen einer Reihe von Energieniveaus innerhalb des Schalenmodells des Kerns; Gefüllte Schalen, wie die gefüllte Schale mit 50 Protonen für Zinn, verleihen dem Nuklid eine ungewöhnliche Stabilität. Of the 254 known stable nuclides, only four have both an odd number of protons and odd number of neutrons: hydrogen-2 (deuterium), lithium-6, boron-10 and nitrogen-14. Also, only four naturally occurring, radioactive odd–odd nuclides have a half-life over a billion years: potassium-40, vanadium-50, lanthanum-138 and tantalum-180m. Most odd–odd nuclei are highly unstable with respect to beta decay, because the decay products are even–even, and are therefore more strongly bound, due to nuclear pairing effects.[61][page needed]
Mass
The large majority of an atom's mass comes from the protons and neutrons that make it up. The total number of these particles (called "nucleons") in a given atom is called the mass number. It is a positive integer and dimensionless (instead of having dimension of mass), because it expresses a count. An example of use of a mass number is "carbon-12," which has 12 nucleons (six protons and six neutrons).
The actual mass of an atom at rest is often expressed using the unified atomic mass unit (u), also called dalton (Da). This unit is defined as a twelfth of the mass of a free neutral atom of carbon-12, which is approximately 1.66×10−27 kg.[62]Hydrogen-1 (the lightest isotope of hydrogen which is also the nuclide with the lowest mass) has an atomic weight of 1.007825 u.[63] The value of this number is called the atomic mass. A given atom has an atomic mass approximately equal (within 1%) to its mass number times the atomic mass unit (for example the mass of a nitrogen-14 is roughly 14 u). However, this number will not be exactly an integer except in the case of carbon-12 (see below).[64] The heaviest stable atom is lead-208,[57] with a mass of 207.9766521 u.[65]
As even the most massive atoms are far too light to work with directly, chemists instead use the unit of moles. One mole of atoms of any element always has the same number of atoms (about 6.022×1023). This number was chosen so that if an element has an atomic mass of 1 u, a mole of atoms of that element has a mass close to one gram. Because of the definition of the unified atomic mass unit, each carbon-12 atom has an atomic mass of exactly 12 u, and so a mole of carbon-12 atoms weighs exactly 0.012 kg.[62]
Shape and size
Atoms lack a well-defined outer boundary, so their dimensions are usually described in terms of an atomic radius. This is a measure of the distance out to which the electron cloud extends from the nucleus.[66] However, this assumes the atom to exhibit a spherical shape, which is only obeyed for atoms in vacuum or free space. Atomic radii may be derived from the distances between two nuclei when the two atoms are joined in a chemical bond. The radius varies with the location of an atom on the atomic chart, the type of chemical bond, the number of neighboring atoms (coordination number) and a quantum mechanical property known as spin.[67] On the periodic table of the elements, atom size tends to increase when moving down columns, but decrease when moving across rows (left to right).[68] Consequently, the smallest atom is helium with a radius of 32 pm, while one of the largest is caesium at 225 pm.[69]
When subjected to external forces, like electrical fields, the shape of an atom may deviate from spherical symmetry. The deformation depends on the field magnitude and the orbital type of outer shell electrons, as shown by group-theoretical considerations. Aspherical deviations might be elicited for instance in crystals, where large crystal-electrical fields may occur at low-symmetry lattice sites.[70][71] Significant ellipsoidal deformations have been shown to occur for sulfur ions[72] and chalcogen ions[73] in pyrite-type compounds.
Atomic dimensions are thousands of times smaller than the wavelengths of light (400–700 nm) so they cannot be viewed using an optical microscope. However, individual atoms can be observed using a scanning tunneling microscope. To visualize the minuteness of the atom, consider that a typical human hair is about 1 million carbon atoms in width.[74] A single drop of water contains about 2 sextillion (2×1021) atoms of oxygen, and twice the number of hydrogen atoms.[75] A single carat diamond with a mass of 2×10−4 kg contains about 10 sextillion (1022) atoms of carbon.[note 2] If an apple were magnified to the size of the Earth, then the atoms in the apple would be approximately the size of the original apple.[76]
Radioactive decay

Every element has one or more isotopes that have unstable nuclei that are subject to radioactive decay, causing the nucleus to emit particles or electromagnetic radiation. Radioactivity can occur when the radius of a nucleus is large compared with the radius of the strong force, which only acts over distances on the order of 1 fm.[77]
The most common forms of radioactive decay are:[78][79]
- Alpha decay: this process is caused when the nucleus emits an alpha particle, which is a helium nucleus consisting of two protons and two neutrons. The result of the emission is a new element with a lower atomic number.
- Beta decay (and electron capture): these processes are regulated by the weak force, and result from a transformation of a neutron into a proton, or a proton into a neutron. The neutron to proton transition is accompanied by the emission of an electron and an antineutrino, while proton to neutron transition (except in electron capture) causes the emission of a positron and a neutrino. The electron or positron emissions are called beta particles. Beta decay either increases or decreases the atomic number of the nucleus by one. Electron capture is more common than positron emission, because it requires less energy. In this type of decay, an electron is absorbed by the nucleus, rather than a positron emitted from the nucleus. A neutrino is still emitted in this process, and a proton changes to a neutron.
- Gamma decay: this process results from a change in the energy level of the nucleus to a lower state, resulting in the emission of electromagnetic radiation. The excited state of a nucleus which results in gamma emission usually occurs following the emission of an alpha or a beta particle. Thus, gamma decay usually follows alpha or beta decay.
Other more rare types of radioactive decay include ejection of neutrons or protons or clusters of nucleons from a nucleus, or more than one beta particle. An analog of gamma emission which allows excited nuclei to lose energy in a different way, is internal conversion—a process that produces high-speed electrons that are not beta rays, followed by production of high-energy photons that are not gamma rays. A few large nuclei explode into two or more charged fragments of varying masses plus several neutrons, in a decay called spontaneous nuclear fission.
Each radioactive isotope has a characteristic decay time period—the half-life—that is determined by the amount of time needed for half of a sample to decay. This is an exponential decay process that steadily decreases the proportion of the remaining isotope by 50% every half-life. Hence after two half-lives have passed only 25% of the isotope is present, and so forth.[77]
Magnetic moment
Elementary particles possess an intrinsic quantum mechanical property known as spin. This is analogous to the angular momentum of an object that is spinning around its center of mass, although strictly speaking these particles are believed to be point-like and cannot be said to be rotating. Spin is measured in units of the reduced Planck constant (ħ), with electrons, protons and neutrons all having spin ½ ħ, or "spin-½". In an atom, electrons in motion around the nucleus possess orbital angular momentum in addition to their spin, while the nucleus itself possesses angular momentum due to its nuclear spin.[80]
The magnetic field produced by an atom—its magnetic moment—is determined by these various forms of angular momentum, just as a rotating charged object classically produces a magnetic field. However, the most dominant contribution comes from electron spin. Due to the nature of electrons to obey the Pauli exclusion principle, in which no two electrons may be found in the same quantum state, bound electrons pair up with each other, with one member of each pair in a spin up state and the other in the opposite, spin down state. Thus these spins cancel each other out, reducing the total magnetic dipole moment to zero in some atoms with even number of electrons.[81]
In ferromagnetic elements such as iron, cobalt and nickel, an odd number of electrons leads to an unpaired electron and a net overall magnetic moment. The orbitals of neighboring atoms overlap and a lower energy state is achieved when the spins of unpaired electrons are aligned with each other, a spontaneous process known as an exchange interaction. When the magnetic moments of ferromagnetic atoms are lined up, the material can produce a measurable macroscopic field. Paramagnetic materials have atoms with magnetic moments that line up in random directions when no magnetic field is present, but the magnetic moments of the individual atoms line up in the presence of a field.[81][82]
The nucleus of an atom will have no spin when it has even numbers of both neutrons and protons, but for other cases of odd numbers, the nucleus may have a spin. Normally nuclei with spin are aligned in random directions because of thermal equilibrium. However, for certain elements (such as xenon-129) it is possible to polarize a significant proportion of the nuclear spin states so that they are aligned in the same direction—a condition called hyperpolarization. This has important applications in magnetic resonance imaging.[83][84]
Energy levels

The potential energy of an electron in an atom is negative, its dependence of its position reaches the minimum (the most absolute value) inside the nucleus, and vanishes when the distance from the nucleus goes to infinity, roughly in an inverse proportion to the distance. In the quantum-mechanical model, a bound electron can only occupy a set of states centered on the nucleus, and each state corresponds to a specific energy level; see time-independent Schrödinger equation for theoretical explanation. An energy level can be measured by the amount of energy needed to unbind the electron from the atom, and is usually given in units of electronvolts (eV). The lowest energy state of a bound electron is called the ground state, i.e. stationary state, while an electron transition to a higher level results in an excited state.[85] The electron's energy raises when n increases because the (average) distance to the nucleus increases. Dependence of the energy on ℓ is caused not by electrostatic potential of the nucleus, but by interaction between electrons.
For an electron to transition between two different states, e.g. grounded state to first excited level (ionization), it must absorb or emit a photon at an energy matching the difference in the potential energy of those levels, according to Niels Bohr model, what can be precisely calculated by the Schrödinger equation.
Electrons jump between orbitals in a particle-like fashion. For example, if a single photon strikes the electrons, only a single electron changes states in response to the photon; see Electron properties.
The energy of an emitted photon is proportional to its frequency, so these specific energy levels appear as distinct bands in the electromagnetic spectrum.[86] Each element has a characteristic spectrum that can depend on the nuclear charge, subshells filled by electrons, the electromagnetic interactions between the electrons and other factors.[87]

When a continuous spectrum of energy is passed through a gas or plasma, some of the photons are absorbed by atoms, causing electrons to change their energy level. Those excited electrons that remain bound to their atom spontaneously emit this energy as a photon, traveling in a random direction, and so drop back to lower energy levels. Thus the atoms behave like a filter that forms a series of dark absorption bands in the energy output. (An observer viewing the atoms from a view that does not include the continuous spectrum in the background, instead sees a series of emission lines from the photons emitted by the atoms.) Spectroscopic measurements of the strength and width of atomic spectral lines allow the composition and physical properties of a substance to be determined.[88]
Close examination of the spectral lines reveals that some display a fine structure splitting. This occurs because of spin–orbit coupling, which is an interaction between the spin and motion of the outermost electron.[89] When an atom is in an external magnetic field, spectral lines become split into three or more components; a phenomenon called the Zeeman effect. This is caused by the interaction of the magnetic field with the magnetic moment of the atom and its electrons. Some atoms can have multiple electron configurations with the same energy level, which thus appear as a single spectral line. The interaction of the magnetic field with the atom shifts these electron configurations to slightly different energy levels, resulting in multiple spectral lines.[90] The presence of an external electric field can cause a comparable splitting and shifting of spectral lines by modifying the electron energy levels, a phenomenon called the Stark effect.[91]
If a bound electron is in an excited state, an interacting photon with the proper energy can cause stimulated emission of a photon with a matching energy level. For this to occur, the electron must drop to a lower energy state that has an energy difference matching the energy of the interacting photon. The emitted photon and the interacting photon then move off in parallel and with matching phases. That is, the wave patterns of the two photons are synchronized. This physical property is used to make lasers, which can emit a coherent beam of light energy in a narrow frequency band.[92]
Valence and bonding behavior
Valency is the combining power of an element. It is equal to number of hydrogen atoms that atom can combine or displace in forming compounds.[93] The outermost electron shell of an atom in its uncombined state is known as the valence shell, and the electrons in
that shell are called valence electrons. The number of valence electrons determines the bonding
behavior with other atoms. Atoms tend to chemically react with each other in a manner that fills (or empties) their outer valence shells.[94] For example, a transfer of a single electron between atoms is a useful approximation for bonds that form between atoms with one-electron more than a filled shell, and others that are one-electron short of a full shell, such as occurs in the compound sodium chloride and other chemical ionic salts. However, many elements display multiple valences, or tendencies to share differing numbers of electrons in different compounds. Thus, chemical bonding between these elements takes many forms of electron-sharing that are more than simple electron transfers. Examples include the element carbon and the organic compounds.[95]
The chemical elements are often displayed in a periodic table that is laid out to display recurring chemical properties, and elements with the same number of valence electrons form a group that is aligned in the same column of the table. (The horizontal rows correspond to the filling of a quantum shell of electrons.) The elements at the far right of the table have their outer shell completely filled with electrons, which results in chemically inert elements known as the noble gases.[96][97]
States

Quantities of atoms are found in different states of matter that depend on the physical conditions, such as temperature and pressure. By varying the conditions, materials can transition between solids, liquids, gases and plasmas.[98] Within a state, a material can also exist in different allotropes. An example of this is solid carbon, which can exist as graphite or diamond.[99] Gaseous allotropes exist as well, such as dioxygen and ozone.
At temperatures close to absolute zero, atoms can form a Bose–Einstein condensate, at which point quantum mechanical effects, which are normally only observed at the atomic scale, become apparent on a macroscopic scale.[100][101] This super-cooled collection of atoms
then behaves as a single super atom, which may allow fundamental checks of quantum mechanical behavior.[102]
Identification

The scanning tunneling microscope is a device for viewing surfaces at the atomic level. It uses the quantum tunneling phenomenon, which allows particles to pass through a barrier that would normally be insurmountable. Electrons tunnel through the vacuum between two planar metal electrodes, on each of which is an adsorbed atom, providing a tunneling-current density that can be measured. Scanning one atom (taken as the tip) as it moves past the other (the sample) permits plotting of tip displacement versus lateral separation for a constant current. The calculation shows the extent to which scanning-tunneling-microscope images of an individual atom are visible. It confirms that for low bias, the microscope images the space-averaged dimensions of the electron orbitals across closely packed energy levels—the Fermi level local density of states.[103][104]
An atom can be ionized by removing one of its electrons. The electric charge causes the trajectory of an atom to bend when it passes through a magnetic field. The radius by which the trajectory of a moving ion is turned by the magnetic field is determined by the mass of the atom. The mass spectrometer uses this principle to measure the mass-to-charge ratio of ions. If a sample contains multiple isotopes, the mass spectrometer can determine the proportion of each isotope in the sample by measuring the intensity of the different beams of ions. Techniques to vaporize atoms include inductively coupled plasma atomic emission spectroscopy and inductively coupled plasma mass spectrometry, both of which use a plasma to vaporize samples for analysis.[105]
A more area-selective method is electron energy loss spectroscopy, which measures the energy loss of an electron beam within a transmission electron microscope when it interacts with a portion of a sample. The atom-probe tomograph has sub-nanometer resolution in 3-D and can chemically identify individual atoms using time-of-flight mass spectrometry.[106]
Spectra of excited states can be used to analyze the atomic composition of distant stars. Specific light wavelengths contained in the observed light from stars can be separated out and related to the quantized transitions in free gas atoms. These colors can be replicated using a gas-discharge lamp containing the same element.[107]Helium was discovered in this way in the spectrum of the Sun 23 years before it was found on Earth.[108]
Origin and current state
Atoms form about 4% of the total energy density of the observable Universe, with an average density of about 0.25 atoms/m3.[109] Within a galaxy such as the Milky Way, atoms have a much higher concentration, with the density of matter in the interstellar medium (ISM) ranging from 105 to 109 atoms/m3.[110] The Sun is believed to be inside the Local Bubble, a region of highly ionized gas, so the density in the solar neighborhood is only about 103 atoms/m3.[111] Stars form from dense clouds in the ISM, and the evolutionary processes of stars result in the steady enrichment of the ISM with elements more massive than hydrogen and helium. Up to 95% of the Milky Way's atoms are concentrated inside stars and the total mass of atoms forms about 10% of the mass of the galaxy.[112] (The remainder of the mass is an unknown dark matter.)[113]
Formation
Electrons are thought to exist in the Universe since early stages of the Big Bang. Atomic nuclei forms in nucleosynthesis reactions. In about three minutes Big Bang nucleosynthesis produced most of the helium, lithium, and deuterium in the Universe, and perhaps some of the beryllium and boron.[114][115][116]
Ubiquitousness and stability of atoms relies on their binding energy, which means that an atom has a lower energy than an unbound system of the nucleus and electrons. Where the temperature is much higher than ionization potential, the matter exists in the form of plasma—a gas of positively charged ions (possibly, bare nuclei) and electrons. When the temperature drops below the ionization potential, atoms become statistically favorable. Atoms (complete with bound electrons) became to dominate over charged particles 380,000 years after the Big Bang—an epoch called recombination, when the expanding Universe cooled enough to allow electrons to become attached to nuclei.[117]
Since the Big Bang, which produced no carbon or heavier elements, atomic nuclei have been combined in stars through the process of nuclear fusion to produce more of the element helium, and (via the triple alpha process) the sequence of elements from carbon up to iron;[118] see stellar nucleosynthesis for details.
Isotopes such as lithium-6, as well as some beryllium and boron are generated in space through cosmic ray spallation.[119] This occurs when a high-energy proton strikes an atomic nucleus, causing large numbers of nucleons to be ejected.
Elements heavier than iron were produced in supernovae through the r-process and in AGB stars through the s-process, both of which involve the capture of neutrons by atomic nuclei.[120] Elements such as lead formed largely through the radioactive decay of heavier elements.[121]
Earth
Most of the atoms that make up the Earth and its inhabitants were present in their current form in the nebula that collapsed out of a molecular cloud to form the Solar System. The rest are the result of radioactive decay, and their relative proportion can be used to determine the age of the Earth through radiometric dating.[123] Most of the helium in the crust of the Earth (about 99% of the helium from gas wells, as shown by its lower abundance of helium-3) is a product of alpha decay.[124]
There are a few trace atoms on Earth that were not present at the beginning (i.e., not "primordial"), nor are results of radioactive decay. Carbon-14 is continuously generated by cosmic rays in the atmosphere.[125] Some atoms on Earth have been artificially generated either deliberately or as by-products of nuclear reactors or explosions.[126][127] Of the transuranic elements—those with atomic numbers greater than 92—only plutonium and neptunium occur naturally on Earth.[128][129] Transuranic elements have radioactive lifetimes shorter than the current age of the Earth[130] and thus identifiable quantities of these elements have long since decayed, with the exception of traces of plutonium-244 possibly deposited by cosmic dust. Natural deposits of plutonium and neptunium are produced by neutron capture in uranium ore.[131]
The Earth contains approximately 1.33×1050 atoms.[132] Although small numbers of independent atoms of noble gases exist, such as argon, neon, and helium, 99% of the atmosphere is bound in the form of molecules, including carbon dioxide and diatomic oxygen and nitrogen. At the surface of the Earth, an overwhelming majority of atoms combine to form various compounds, including water, salt, silicates and oxides. Atoms can also combine to create materials that do not consist of discrete molecules, including crystals and liquid or solid metals.[133][134] This atomic matter forms networked arrangements that lack the particular type of small-scale interrupted order associated with molecular matter.[135]
Rare and theoretical forms
Superheavy elements
While isotopes with atomic numbers higher than lead (82) are known to be radioactive, an "island of stability" has been proposed for some elements with atomic numbers above 103. These superheavy elements may have a nucleus that is relatively stable against radioactive decay.[136] The most likely candidate for a stable superheavy atom, unbihexium, has 126 protons and 184 neutrons.[137]
Exotic matter
Each particle of matter has a corresponding antimatter particle with the opposite electrical charge. Thus, the positron is a positively charged antielectron and the antiproton is a negatively charged equivalent of a proton. When a matter and corresponding antimatter particle meet, they annihilate each other. Because of this, along with an imbalance between the number of matter and antimatter particles, the latter are rare in the universe. The first causes of this imbalance are not yet fully understood, although theories of baryogenesis may offer an explanation. As a result, no antimatter atoms have been discovered in nature.[138][139] However, in 1996 the antimatter counterpart of the hydrogen atom (antihydrogen) was synthesized at the CERN laboratory in Geneva.[140][141]
Other exotic atoms have been created by replacing one of the protons, neutrons or electrons with other particles that have the same charge. For example, an electron can be replaced by a more massive muon, forming a muonic atom. These types of atoms can be used to test the fundamental predictions of physics.[142][143][144]
See also
Notes
References
- ^ Pullman, Bernard (1998). The Atom in the History of Human Thought. Oxford, England: Oxford University Press. S. 31–33. ISBN 978-0-19-515040-7.
- ^ a b Kenny, Anthony (2004). Ancient Philosophy. Eine neue Geschichte der westlichen Philosophie. 1. Oxford, England: Oxford University Press. S. 26–28. ISBN 978-0-19-875273-8.
- ^ a b c d e f g h i j Pyle, Andrew (2010). "Atome und Atomismus". In Grafton Anthony; Die meisten Glenn W .; Settis, Salvatore. The Classical Tradition. Cambridge, Massachusetts and London: The Belknap Press of Harvard University Press. S. 103–104. ISBN 978-0-674-03572-0.
- ^ a b c d Cohen, Henri; Lefebvre, Claire, Hrsg. (2017). Handbook of Categorization in Cognitive Science (Second ed.). Amsterdam, Niederlande: Elsevier. p. 427. ISBN 978-0-08-101107-2.
- ^ Andrew G. van Melsen (1952). From Atomos to Atom. Mineola, NY: Dover-Veröffentlichungen. ISBN 978-0-486-49584-2.
- ^ Dalton, John. "On the Absorption of Gases by Water and Other Liquids", in Memoirs of the Literary and Philosophical Society of Manchester. 1803. Retrieved on August 29, 2007.
- ^ Einstein, Albert (1905). "Über die von der molekularkinetischen Theorie der Wärme geforderte Bewegung von in ruhenden Flüssigkeiten suspendierten Teilchen" (PDF). Annalen der Physik (in German). 322 (8): 549–560. Bibcode: 1905AnP ... 322..549E. doi:10.1002/andp.19053220806. Retrieved 4 February 2007.
- ^ Mazo, Robert M. (2002). Brownian Motion: Fluctuations, Dynamics, and Applications. Oxford University Press. pp. 1–7. ISBN 978-0-19-851567-8. OCLC 48753074.
- ^ Lee, Y.K.; Hoon, K. (1995). "Brownian Motion". Imperial College. Archived from the original on 18 December 2007. Retrieved 18 December 2007.
- ^ Patterson, G. (2007). "Jean Perrin and the triumph of the atomic doctrine". Endeavour. 31 (2): 50–53. doi:10.1016/j.endeavour.2007.05.003. PMID 17602746.
- ^ Thomson, J.J. (August 1901). "On bodies smaller than atoms". The Popular Science Monthly: 323–335. Retrieved 2009-06-21.
- ^ "J.J. Thomson". Nobel-Stiftung 1906. Retrieved 20 December 2007.
- ^ Rutherford, E. (1911). "The Scattering of α and β Particles by Matter and the Structure of the Atom" (PDF). Philosophical Magazine. 21 (125): 669–688. doi:10.1080/14786440508637080.
- ^ "Frederick Soddy, The Nobel Prize in Chemistry 1921". Nobel Foundation. Retrieved 18 January 2008.
- ^ Thomson, Joseph John (1913). "Strahlen von positiver Elektrizität". Proceedings of the Royal Society. A. 89 (607): 1–20. Bibcode: 1913RSPSA..89 .... 1T. doi:10.1098/rspa.1913.0057.
- ^ Stern, David P. (16 May 2005). "The Atomic Nucleus and Bohr's Early Model of the Atom". NASA/Goddard Space Flight Center. Retrieved 20 December 2007.
- ^ Bohr, Niels (11 December 1922). "Niels Bohr, The Nobel Prize in Physics 1922, Nobel Lecture". Nobel Foundation. Retrieved 16 February 2008.
- ^ a b c Pais, Abraham (1986). Inward Bound: Of Matter and Forces in the Physical World. New York: Oxford University Press. pp. 228–230. ISBN 978-0-19-851971-3.
- ^ Lewis, Gilbert N. (1916). "The Atom and the Molecule". Journal of the American Chemical Society. 38 (4): 762–786. doi:10.1021/ja02261a002.
- ^ Scerri, Eric R. (2007). The periodic table: its story and its significance. Oxford University Press US. pp. 205–226. ISBN 978-0-19-530573-9.
- ^ Langmuir, Irving (1919). "The Arrangement of Electrons in Atoms and Molecules". Journal of the American Chemical Society. 41 (6): 868–934. doi:10.1021/ja02227a002.
- ^ Scully, Marlan O.; Lamb, Willis E.; Barut, Asim (1987). "On the theory of the Stern-Gerlach apparatus". Foundations of Physics. 17 (6): 575–583. Bibcode:1987FoPh...17..575S. doi:10.1007/BF01882788.
- ^ Chad Orzel (16 September 2014). "What is the Heisenberg Uncertainty Principle?". TED-Ed – via YouTube.
- ^ Brown, Kevin (2007). "The Hydrogen Atom". MathPages. Retrieved 21 December 2007.
- ^ Harrison, David M. (2000). "The Development of Quantum Mechanics". University of Toronto. Archived from the original on 25 December 2007. Retrieved 21 December 2007.
- ^ Aston, Francis W. (1920). "The constitution of atmospheric neon". Philosophical Magazine. 39 (6): 449–455. doi:10.1080/14786440408636058.
- ^ Chadwick, James (12 December 1935). "Nobel Lecture: The Neutron and Its Properties". Nobel Foundation. Retrieved 21 December 2007.
- ^ Bowden, Mary Ellen (1997). "Otto Hahn, Lise Meitner, and Fritz Strassmann". Chemical achievers : the human face of the chemical sciences. Philadelphia, PA: Chemical Heritage Foundation. pp. 76–80, 125. ISBN 978-0-941901-12-3.
- ^ "Otto Hahn, Lise Meitner, and Fritz Strassmann". Science History Institute. June 2016. Retrieved 20 March 2018.
- ^ Meitner, Lise; Frisch, Otto Robert (1939). "Disintegration of uranium by neutrons: a new type of nuclear reaction". Nature. 143 (3615): 239–240. Bibcode:1939Natur.143..239M. doi:10.1038/143239a0.
- ^ Schroeder, M. "Lise Meitner – Zur 125. Wiederkehr Ihres Geburtstages" (in German). Archived from the original on 19 July 2011. Retrieved 4 June 2009.
- ^ Crawford, E.; Sime, Ruth Lewin; Walker, Mark (1997). "A Nobel tale of postwar injustice". Physics Today. 50 (9): 26–32. Bibcode:1997PhT....50i..26C. doi:10.1063/1.881933.
- ^ Kullander, Sven (28 August 2001). "Accelerators and Nobel Laureates". Nobel Foundation. Retrieved 31 January 2008.
- ^ "The Nobel Prize in Physics 1990". Nobel-Stiftung 17 October 1990. Retrieved 31 January 2008.
- ^ Demtröder, Wolfgang (2002). Atoms, Molecules and Photons: An Introduction to Atomic- Molecular- and Quantum Physics (1st ed.). Springer pp. 39–42. ISBN 978-3-540-20631-6. OCLC 181435713.
- ^ Woan, Graham (2000). The Cambridge Handbook of Physics. Cambridge University Press. p. 8. ISBN 978-0-521-57507-2. OCLC 224032426.
- ^ MacGregor, Malcolm H. (1992). The Enigmatic Electron. Oxford University Press. pp. 33–37. ISBN 978-0-19-521833-6. OCLC 223372888.
- ^ a b Particle Data Group (2002). "The Particle Adventure". Lawrence Berkeley Laboratory. Archived from the original on 4 January 2007. Retrieved 3 January 2007.
- ^ a b Schombert, James (18 April 2006). "Elementary Particles". University of Oregon. Retrieved 3 January 2007.
- ^ Jevremovic, Tatjana (2005). Nuclear Principles in Engineering. Springer p. 63. ISBN 978-0-387-23284-3. OCLC 228384008.
- ^ Pfeffer, Jeremy I.; Nir, Shlomo (2000). Modern Physics: An Introductory Text. Imperial College Press. pp. 330–336. ISBN 978-1-86094-250-1. OCLC 45900880.
- ^ Wenner, Jennifer M. (10 October 2007). "How Does Radioactive Decay Work?". Carleton College. Retrieved 9 January 2008.
- ^ a b c Raymond, David (7 April 2006). "Nuclear Binding Energies". New Mexico Tech. Archived from the original on 1 December 2002. Retrieved 3 January 2007.
- ^ Mihos, Chris (23 July 2002). "Overcoming the Coulomb Barrier". Case Western Reserve University. Retrieved 13 February 2008.
- ^ Staff (30 March 2007). "ABC's of Nuclear Science". Lawrence Berkeley National Laboratory. Archived from the original on 5 December 2006. Retrieved 3 January 2007.
- ^ Makhijani, Arjun; Saleska, Scott (2 March 2001). "Basics of Nuclear Physics and Fission". Institute for Energy and Environmental Research. Archived from the original on 16 January 2007. Retrieved 3 January 2007.
- ^ Shultis, J. Kenneth; Faw, Richard E. (2002). Fundamentals of Nuclear Science and Engineering. CRC Press. pp. 10–17. ISBN 978-0-8247-0834-4. OCLC 123346507.
- ^ Fewell, M.P. (1995). "The atomic nuclide with the highest mean binding energy". American Journal of Physics. 63 (7): 653–658. Bibcode:1995AmJPh..63..653F. doi:10.1119/1.17828.
- ^ Mulliken, Robert S. (1967). "Spectroscopy, Molecular Orbitals, and Chemical Bonding". Science. 157 (3784): 13–24. Bibcode:1967Sci...157...13M. doi:10.1126/science.157.3784.13. PMID 5338306.
- ^ a b Brucat, Philip J. (2008). "The Quantum Atom". University of Florida. Archived from the original on 7 December 2006. Retrieved 4 January 2007.
- ^ Manthey, David (2001). "Atomic Orbitals". Orbital Central. Archived from the original on 10 January 2008. Retrieved 21 January 2008.
- ^ Herter, Terry (2006). "Lecture 8: The Hydrogen Atom". Cornell Universität. Archived from the original on 22 February 2012. Retrieved 14 February 2008.
- ^ Bell, R.E.; Elliott, L.G. (1950). "Gamma-Rays from the Reaction H1(n,γ)D2 and the Binding Energy of the Deuteron". Physical Review. 79 (2): 282–285. Bibcode:1950PhRv...79..282B. doi:10.1103/PhysRev.79.282.
- ^ Smirnov, Boris M. (2003). Physics of Atoms and Ions. Springer pp. 249–272. ISBN 978-0-387-95550-6.
- ^ Matis, Howard S. (9 August 2000). "The Isotopes of Hydrogen". Guide to the Nuclear Wall Chart. Lawrence Berkeley National Lab. Archived from the original on 18 December 2007. Retrieved 21 December 2007.
- ^ Weiss, Rick (17 October 2006). "Scientists Announce Creation of Atomic Element, the Heaviest Yet". Washington Post. Retrieved 21 December 2007.
- ^ a b Sills, Alan D. (2003). Earth Science the Easy Way. Barrons Bildungsserie. pp. 131–134. ISBN 978-0-7641-2146-3. OCLC 51543743.
- ^ Dumé, Belle (23 April 2003). "Bismuth breaks half-life record for alpha decay". Physics World. Archived from the original on 14 December 2007. Retrieved 21 December 2007.
- ^ Lindsay, Don (30 July 2000). "Radioactives Missing From The Earth". Don Lindsay Archive. Archived from the original on 28 April 2007. Retrieved 23 May 2007.
- ^ Tuli, Jagdish K. (April 2005). "Nuclear Wallet Cards". National Nuclear Data Center, Brookhaven National Laboratory. Retrieved 16 April 2011.
- ^ a b CRC Handbook (2002).
- ^ a b Mills, Ian; Cvitaš, Tomislav; Homann, Klaus; Kallay, Nikola; Kuchitsu, Kozo (1993). Quantities, Units and Symbols in Physical Chemistry (PDF) (2nd ed.). Oxford: International Union of Pure and Applied Chemistry, Commission on Physiochemical Symbols Terminology and Units, Blackwell Scientific Publications. p. 70. ISBN 978-0-632-03583-0. OCLC 27011505.
- ^ Chieh, Chung (22 January 2001). "Nuclide Stability". University of Waterloo. Archived from the original on 30 August 2007. Retrieved 4 January 2007.
- ^ "Atomic Weights and Isotopic Compositions for All Elements". Nationales Institut für Standards und Technologie. Archived from the original on 31 December 2006. Retrieved 4 January 2007.
- ^ Audi, G.; Wapstra, A.H.; Thibault, C. (2003). "The Ame2003 atomic mass evaluation (II)" (PDF). Nuclear Physics A. 729 (1): 337–676. Bibcode:2003NuPhA.729..337A. doi:10.1016/j.nuclphysa.2003.11.003.
- ^ Ghosh, D.C.; Biswas, R. (2002). "Theoretical calculation of Absolute Radii of Atoms and Ions. Part 1. The Atomic Radii". Int. J. Mol. Sci. 3 (11): 87–113. doi:10.3390/i3020087.
- ^ Shannon, R.D. (1976). "Revised effective ionic radii and systematic studies of interatomic distances in halides and chalcogenides". Acta Crystallographica A. 32 (5): 751–767. Bibcode:1976AcCrA..32..751S. doi:10.1107/S0567739476001551.
- ^ Dong, Judy (1998). "Diameter of an Atom". The Physics Factbook. Archived from the original on 4 November 2007. Retrieved 19 November 2007.
- ^ Zumdahl, Steven S. (2002). Introductory Chemistry: A Foundation (5th ed.). Houghton Mifflin. ISBN 978-0-618-34342-3. OCLC 173081482. Archived from the original on 4 March 2008. Retrieved 5 February 2008.
- ^ Bethe, Hans (1929). "Termaufspaltung in Kristallen". Annalen der Physik. 3 (2): 133–208. Bibcode:1929AnP...395..133B. doi:10.1002/andp.19293950202.
- ^ Birkholz, Mario (1995). "Crystal-field induced dipoles in heteropolar crystals – I. concept". Z. Phys. B. 96 (3): 325–332. Bibcode:1995ZPhyB..96..325B. CiteSeerX 10.1.1.424.5632. doi:10.1007/BF01313054.
- ^ Birkholz, M.; Rudert, R. (2008). "Interatomic distances in pyrite-structure disulfides – a case for ellipsoidal modeling of sulfur ions]". Physica Status Solidi B. 245 (9): 1858–1864. Bibcode:2008PSSBR.245.1858B. doi:10.1002/pssb.200879532.
- ^ Birkholz, M. (2014). "Modeling the Shape of Ions in Pyrite-Type Crystals". Crystals. 4 (4): 390–403. doi:10.3390/cryst4030390.
- ^ Staff (2007). "Small Miracles: Harnessing nanotechnology". Oregon State University. Retrieved 7 January 2007. – describes the width of a human hair as 105 nm and 10 carbon atoms as spanning 1 nm.
- ^ Padilla, Michael J.; Miaoulis, Ioannis; Cyr, Martha (2002). Prentice Hall Science Explorer: Chemical Building Blocks. Upper Saddle River, New Jersey: Prentice-Hall, Inc. p. 32. ISBN 978-0-13-054091-1. OCLC 47925884.
There are 2,000,000,000,000,000,000,000 (that's 2 sextillion) atoms of oxygen in one drop of water—and twice as many atoms of hydrogen.
- ^ Feynman, Richard (1995). Six Easy Pieces. The Penguin Group. p. 5. ISBN 978-0-14-027666-4. OCLC 40499574.
- ^ a b "Radioactivity". Splung.com. Archived from the original on 4 December 2007. Retrieved 19 December 2007.
- ^ L'Annunziata, Michael F. (2003). Handbook of Radioactivity Analysis. Akademische Presse. pp. 3–56. ISBN 978-0-12-436603-9. OCLC 16212955.
- ^ Firestone, Richard B. (22 May 2000). "Radioactive Decay Modes". Berkeley Laboratory. Archived from the original on 29 September 2006. Retrieved 7 January 2007.
- ^ Hornak, J.P. (2006). "Chapter 3: Spin Physics". The Basics of NMR. Rochester Institute of Technology. Archived from the original on 3 February 2007. Retrieved 7 January 2007.
- ^ a b Schroeder, Paul A. (25 February 2000). "Magnetic Properties". Universität von Georgia. Archived from the original on 29 April 2007. Retrieved 7 January 2007.
- ^ Goebel, Greg (1 September 2007). "[4.3] Magnetic Properties of the Atom". Elementary Quantum Physics. In The Public Domain website. Archived from the original on 21 August 2011. Retrieved 7 January 2007.
- ^ Yarris, Lynn (Spring 1997). "Talking Pictures". Berkeley Lab Research Review. Archived from the original on 13 January 2008. Retrieved 9 January 2008.
- ^ Liang, Z.-P.; Haacke, E.M. (1999). Webster, J.G., ed. Encyclopedia of Electrical and Electronics Engineering: Magnetic Resonance Imaging. vol. 2. John Wiley & Sons. pp. 412–426. ISBN 978-0-471-13946-1.
- ^ Zeghbroeck, Bart J. Van (1998). "Energy levels". Shippensburg University. Archived from the original on 15 January 2005. Retrieved 23 December 2007.
- ^ Fowles, Grant R. (1989). Introduction to Modern Optics. Courier Dover Publikationen. pp. 227–233. ISBN 978-0-486-65957-2. OCLC 18834711.
- ^ Martin, W.C.; Wiese, W.L. (Mai 2007). "Atomic Spectroscopy: A Compendium of Basic Ideas, Notation, Data, and Formulas". Nationales Institut für Standards und Technologie. Archived from the original on 8 February 2007. Retrieved 8 January 2007.
- ^ "Atomic Emission Spectra – Origin of Spectral Lines". Avogadro Web Site. Archived from the original on 28 February 2006. Retrieved 10 August 2006.
- ^ Fitzpatrick, Richard (16 February 2007). "Fine structure". University of Texas at Austin. Retrieved 14 February 2008.
- ^ Weiss, Michael (2001). "The Zeeman Effect". University of California-Riverside. Archived from the original on 2 February 2008. Retrieved 6 February 2008.
- ^ Beyer, H.F.; Shevelko, V.P. (2003). Introduction to the Physics of Highly Charged Ions. CRC Press. pp. 232–236. ISBN 978-0-7503-0481-8. OCLC 47150433.
- ^ Watkins, Thayer. "Coherence in Stimulated Emission". San José State University. Archived from the original on 12 January 2008. Retrieved 23 December 2007.
- ^ oxford dictionary – valency
- ^ Reusch, William (16 July 2007). "Virtual Textbook of Organic Chemistry". Michigan State University. Archived from the original on 29 October 2007. Retrieved 11 January 2008.
- ^ "Covalent bonding – Single bonds". chemguide. 2000.
- ^ Husted, Robert; et al. (11 December 2003). "Periodic Table of the Elements". Los Alamos Nationales Labor. Archived from the original on 10 January 2008. Retrieved 11 January 2008.
- ^ Baum, Rudy (2003). "It's Elemental: The Periodic Table". Chemical & Engineering News. Retrieved 11 January 2008.
- ^ Goodstein, David L. (2002). States of Matter. Courier Dover Publikationen. pp. 436–438. ISBN 978-0-13-843557-8.
- ^ Brazhkin, Vadim V. (2006). "Metastable phases, phase transformations, and phase diagrams in physics and chemistry". Physics-Uspekhi. 49 (7): 719–724. Bibcode:2006PhyU...49..719B. doi:10.1070/PU2006v049n07ABEH006013.
- ^ Myers, Richard (2003). The Basics of Chemistry. Greenwood Press. p. 85. ISBN 978-0-313-31664-7. OCLC 50164580.
- ^ Staff (9 October 2001). "Bose-Einstein Condensate: A New Form of Matter". Nationales Institut für Standards und Technologie. Archived from the original on 3 January 2008. Retrieved 16 January 2008.
- ^ Colton, Imogen; Fyffe, Jeanette (3 February 1999). "Super Atoms from Bose-Einstein Condensation". The University of Melbourne. Archived from the original on 29 August 2007. Retrieved 6 February 2008.
- ^ Jacox, Marilyn; Gadzuk, J. William (November 1997). "Scanning Tunneling Microscope". Nationales Institut für Standards und Technologie. Archived from the original on 7 January 2008. Retrieved 11 January 2008.
- ^ "The Nobel Prize in Physics 1986". The Nobel Foundation. Retrieved 11 January 2008. – in particular, see the Nobel lecture by G. Binnig and H. Rohrer.
- ^ Jakubowski, N.; Moens, Luc; Vanhaecke, Frank (1998). "Sector field mass spectrometers in ICP-MS". Spectrochimica Acta Part B: Atomic Spectroscopy. 53 (13): 1739–1763. Bibcode:1998AcSpe..53.1739J. doi:10.1016/S0584-8547(98)00222-5.
- ^ Müller, Erwin W.; Panitz, John A.; McLane, S. Brooks (1968). "The Atom-Probe Field Ion Microscope". Review of Scientific Instruments. 39 (1): 83–86. Bibcode:1968RScI...39...83M. doi:10.1063/1.1683116.
- ^ Lochner, Jim; Gibb, Meredith; Newman, Phil (30 April 2007). "What Do Spectra Tell Us?". NASA/Goddard Space Flight Center. Archived from the original on 16 January 2008. Retrieved 3 January 2008.
- ^ Winter, Mark (2007). "Helium". WebElements. Archived from the original on 30 December 2007. Retrieved 3 January 2008.
- ^ Hinshaw, Gary (10 February 2006). "What is the Universe Made Of?". NASA/WMAP. Archived from the original on 31 December 2007. Retrieved 7 January 2008.
- ^ Choppin, Gregory R.; Liljenzin, Jan-Olov; Rydberg, Jan (2001). Radiochemistry and Nuclear Chemistry. Elsevier p. 441. ISBN 978-0-7506-7463-8. OCLC 162592180.
- ^ Davidsen, Arthur F. (1993). "Far-Ultraviolet Astronomy on the Astro-1 Space Shuttle Mission". Science. 259 (5093): 327–334. Bibcode:1993Sci...259..327D. doi:10.1126/science.259.5093.327. PMID 17832344.
- ^ Lequeux, James (2005). The Interstellar Medium. Springer p. 4. ISBN 978-3-540-21326-0. OCLC 133157789.
- ^ Smith, Nigel (6 January 2000). "The search for dark matter". Physics World. Archived from the original on 16 February 2008. Retrieved 14 February 2008.
- ^ Croswell, Ken (1991). "Boron, bumps and the Big Bang: Was matter spread evenly when the Universe began? Perhaps not; the clues lie in the creation of the lighter elements such as boron and beryllium". New Scientist (1794): 42. Archived from the original on 7 February 2008. Retrieved 14 January 2008.
- ^ Copi, Craig J.; Schramm, DN; Turner, MS (1995). "Big-Bang Nucleosynthesis and the Baryon Density of the Universe". Science (Submitted manuscript). 267 (5195): 192–199. arXiv:astro-ph/9407006. Bibcode:1995Sci...267..192C. doi:10.1126/science.7809624. PMID 7809624.
- ^ Hinshaw, Gary (15 December 2005). "Tests of the Big Bang: The Light Elements". NASA/WMAP. Archived from the original on 17 January 2008. Retrieved 13 January 2008.
- ^ Abbott, Brian (30 May 2007). "Microwave (WMAP) All-Sky Survey". Hayden Planetarium. Archived from the original on 13 February 2013. Retrieved 13 January 2008.
- ^ Hoyle, F. (1946). "The synthesis of the elements from hydrogen". Monthly Notices of the Royal Astronomical Society. 106 (5): 343–383. Bibcode:1946MNRAS.106..343H. doi:10.1093/mnras/106.5.343.
- ^ Knauth, D.C.; Knauth, D.C.; Lambert, David L.; Crane, P. (2000). "Newly synthesized lithium in the interstellar medium". Nature. 405 (6787): 656–658. Bibcode:2000Natur.405..656K. doi:10.1038/35015028. PMID 10864316.
- ^ Mashnik, Stepan G. (2000). "On Solar System and Cosmic Rays Nucleosynthesis and Spallation Processes". arXiv:astro-ph/0008382.
- ^ Kansas Geological Survey (4 May 2005). "Age of the Earth". University of Kansas. Archived from the original on 5 July 2008. Retrieved 14 January 2008.
- ^ Dalrymple, G. Brent (2001). "The age of the Earth in the twentieth century: a problem (mostly) solved". Geological Society, London, Special Publications. 190 (1): 205–221. Bibcode:2001GSLSP.190..205D. doi:10.1144/GSL.SP.2001.190.01.14. Retrieved 14 January 2008.
- ^ Anderson, Don L.; Foulger, G.R.; Meibom, Anders (2 September 2006). "Helium: Fundamental models". MantlePlumes.org. Archived from the original on 8 February 2007. Retrieved 14 January 2007.
- ^ Pennicott, Katie (10 May 2001). "Carbon clock could show the wrong time". PhysicsWeb. Archived from the original on 15 December 2007. Retrieved 14 January 2008.
- ^ Yarris, Lynn (27 July 2001). "New Superheavy Elements 118 and 116 Discovered at Berkeley Lab". Berkeley Lab. Archived from the original on 9 January 2008. Retrieved 14 January 2008.
- ^ Diamond, H; et al. (1960). "Heavy Isotope Abundances in Mike Thermonuclear Device". Physical Review. 119 (6): 2000–2004. Bibcode:1960PhRv..119.2000D. doi:10.1103/PhysRev.119.2000.
- ^ Poston Sr.; John W. (23 March 1998). "Do transuranic elements such as plutonium ever occur naturally?". Scientific American.
- ^ Keller, C. (1973). "Natural occurrence of lanthanides, actinides, and superheavy elements". Chemiker Zeitung. 97 (10): 522–530. OSTI 4353086.
- ^ Zaider, Marco; Rossi, Harald H. (2001). Radiation Science for Physicians and Public Health Workers. Springer p. 17. ISBN 978-0-306-46403-4. OCLC 44110319.
- ^ "Oklo Fossil Reactors". Curtin University of Technology. Archived from the original on 18 December 2007. Retrieved 15 January 2008.
- ^ Weisenberger, Drew. "How many atoms are there in the world?". Jefferson Lab. Retrieved 16 January 2008.
- ^ Pidwirny, Michael. "Fundamentals of Physical Geography". University of British Columbia Okanagan. Archived from the original on 21 January 2008. Retrieved 16 January 2008.
- ^ Anderson, Don L. (2002). "The inner inner core of Earth". Proceedings of the National Academy of Sciences. 99 (22): 13966–13968. Bibcode:2002PNAS...9913966A. doi:10.1073/pnas.232565899. PMC 137819. PMID 12391308.
- ^ Pauling, Linus (1960). The Nature of the Chemical Bond. Cornell University Press. S. 5–10. ISBN 978-0-8014-0333-0. OCLC 17518275.
- ^ Anonymous (2 October 2001). "Second postcard from the island of stability". CERN Courier. Archived from the original on 3 February 2008. Retrieved 14 January 2008.
- ^ Jacoby, Mitch (2006). "As-yet-unsynthesized superheavy atom should form a stable diatomic molecule with fluorine". Chemical & Engineering News. 84 (10): 19. doi:10.1021/cen-v084n010.p019a.
- ^ Koppes, Steve (1 March 1999). "Fermilab Physicists Find New Matter-Antimatter Asymmetry". University of Chicago. Retrieved 14 January 2008.
- ^ Cromie, William J. (16 August 2001). "A lifetime of trillionths of a second: Scientists explore antimatter". Harvard University Gazette. Retrieved 14 January 2008.
- ^ Hijmans, Tom W. (2002). "Particle physics: Cold antihydrogen". Nature. 419 (6906): 439–440. Bibcode:2002Natur.419..439H. doi:10.1038/419439a. PMID 12368837.
- ^ Staff (30 October 2002). "Researchers 'look inside' antimatter". BBC News. Retrieved 14 January 2008.
- ^ Barrett, Roger (1990). "The Strange World of the Exotic Atom". New Scientist (1728): 77–115. Archived from the original on 21 December 2007. Retrieved 4 January 2008.
- ^ Indelicato, Paul (2004). "Exotic Atoms". Physica Scripta. T112 (1): 20–26. arXiv:physics/0409058. Bibcode:2004PhST..112...20I. doi:10.1238/Physica.Topical.112a00020.
- ^ Ripin, Barrett H. (July 1998). "Recent Experiments on Exotic Atoms". American Physical Society. Archived from the original on 2016-05-17. Retrieved 15 February 2008.
Sources
Further reading
- Dalton, J. (1808). A New System of Chemical Philosophy, Part 1. London and Manchester: S. Russell.
- Gangopadhyaya, Mrinalkanti (1981). Indian Atomism: History and Sources. Atlantic Highlands, New Jersey: Humanities Press. ISBN 978-0-391-02177-8. OCLC 10916778.
- Harrison, Edward Robert (2003). Masks of the Universe: Changing Ideas on the Nature of the Cosmos. Cambridge University Press. ISBN 978-0-521-77351-5. OCLC 50441595.
- Iannone, A. Pablo (2001). Dictionary of World Philosophy. Routledge. ISBN 978-0-415-17995-9. OCLC 44541769.
- King, Richard (1999). Indian philosophy: an introduction to Hindu and Buddhist thought. Edinburgh University Press. ISBN 978-0-7486-0954-3.
- Levere, Trevor, H. (2001). Transforming Matter – A History of Chemistry for Alchemy to the Buckyball. The Johns Hopkins University Press. ISBN 978-0-8018-6610-4.
- Liddell, Henry George; Scott, Robert "A Greek-English Lexicon". Perseus Digital Library.
- Liddell, Henry George; Scott, Robert "ἄτομος". A Greek-English Lexicon. Perseus Digital Library. Retrieved 21 June 2010.
- McEvilley, Thomas (2002). The shape of ancient thought: comparative studies in Greek and Indian philosophies. Allworth Press. ISBN 978-1-58115-203-6.
- Moran, Bruce T. (2005). Distilling Knowledge: Alchemy, Chemistry, and the Scientific Revolution. Harvard University Press. ISBN 978-0-674-01495-4.
- Ponomarev, Leonid Ivanovich (1993). The Quantum Dice. CRC Press. ISBN 978-0-7503-0251-7. OCLC 26853108.
- Roscoe, Henry Enfield (1895). John Dalton and the Rise of Modern Chemistry. Century science series. New York: Macmillan. Retrieved 3 April 2011.
- Siegfried, Robert (2002). From Elements to Atoms: A History of Chemical Composition. DIANE. ISBN 978-0-87169-924-4. OCLC 186607849.
- Teresi, Dick (2003). Lost Discoveries: The Ancient Roots of Modern Science. Simon & Schuster pp. 213–214. ISBN 978-0-7432-4379-7.
- Various (2002). Lide, David R., ed. Handbook of Chemistry & Physics (88th ed.). CRC. ISBN 978-0-8493-0486-6. OCLC 179976746. Archived from the original on 23 May 2008. Retrieved 23 May 2008.
- Wurtz, Charles Adolphe (1881). The Atomic Theory. New York: D. Appleton and company. ISBN 978-0-559-43636-9.
No comments:
Post a Comment